利奈唑胺是一种恶唑烷酮类抗生素���,最初用于治疗耐多药革兰阳性菌相关肺炎���、皮肤和软组织感染��,由于其在深部组织的高渗透率���,临床应用逐渐扩展到骨和关节感染���、耐多药结核病等领域���。
但利奈唑胺存在具有量效关系的不良反应���,建议治疗时长不超过 28 天[1]���。有研究表明���,利奈唑胺谷浓度(Cmin)高于 8mg/L 时���,患者发生血小板减少的风险可能增加���。此前在研究中心进行的回顾性分析发现���,接受标准剂量(每 12 小时 600mg)利奈唑胺治疗的患者中���,33.0% 的人Cmin高于上述阈值[2]���。本研究旨在评估主动的 TDM 能否通过优化利奈唑胺暴露量���,预防血小板减少在长期利奈唑胺治疗患者中的发生���。
本研究为收集了2015年-2017年在意大利乌迪内的61例耐多药革兰阳性菌感染成年患者���。患者接收了10天以上利奈唑胺治疗���。患者的利奈唑胺治疗方案为标准的每 12 小时 600mg 剂量���,并可能辅佐其它联合治疗���。治疗过程中监测血小板计数���、血红蛋白浓度���、C 反应蛋白和血清肌酐等指标���,同时采用TDM检测Cmin���,目标是将利奈唑胺Cmin控制在 2 - 8mg/L���。本研究将按照利奈唑胺的暴露情况分为如下组别���:暴露充足稳定(A 组)���、暴露过量(B 组)���,暴露不足(C 组)��。其中B组又分为能通过 TDM 稳定达到目标范围的 B1 亚组和不能达到的 B2 亚组���;C组又分为能达标的C1组和不能达标的C2组���。
试验结束后��,最终纳入的 61 例患者表现为���:A组28 例(45.9%)���,B组33 例(54.1%)(其中 B1 亚组 29 例���,B2 亚组 4 例)���,C 组为0例���。患者以男性为主���,中位年龄 62 岁���,主要感染类型为骨和关节感染���,常见病原菌为耐甲氧西林金黄色葡萄球菌(MRSA)和耐甲氧西林凝固酶阴性葡萄球菌(methicillin-resistant CoNS)��。虽然最初治疗是采用相同策略���,但是在TDM的介入情况下���,A组同B1组的治疗方案有明显差异(17.9 VS 12.8 mg/kg/day���;p<0.001)���,A组与B2组也存在治疗差异(17.9 VS 13.3 mg/kg/day���,p=0.002)���。此外���,A组与 B1或B2 组的Cmin也存在差异(分别为3.8 VS 5.1 mg/L 和 3.8 VS 8.3 mg/L���,p<0.001 )��。
血小板减少发生情况��:总体血小板减少发生率为 14.8%(9/61)���,A 组(10.7%���,3/28)和 B1 亚组(10.3%���,3/29)的发生率显著低于 B2 亚组(75.0%���,3/4)���。其中B1 亚组中发生血小板减少的患者在TDM的指导用药情况下���,并未停药即得以逐渐恢复���,直至治疗计划结束���。
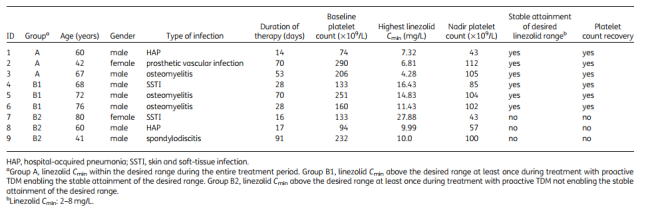
最终患者分组及副作用发生情况如图表1所示���。发生血小板减少患者的参数特征如表格1所示���。

Figure 1. Study flow chart
Table 1. Characteristics of those patients who experienced thrombocytopenia during linezolid treatment (n=9)
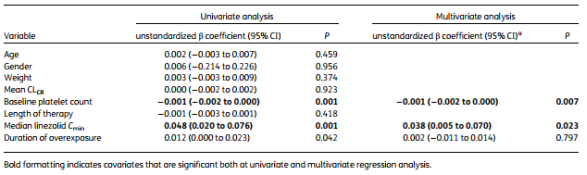
单因素和多因素线性回归分析显示���,血小板减少发生概率独立性的与利奈唑胺谷浓度Cmin和极限血小板技术显著相关(如表格2所示)���。
Table 2. Univariate and multivariate regression analysis of variables associated with the occurrence of thrombocytopenia (n=61 patients)
本研究探讨了积极的TDM对优化利奈唑胺暴露量���,预防和恢复剂量依赖性血小板减少的作用���。利奈唑胺引起的血小板减少是主要不良反应��,可能导致治疗中断���。早期临床试验中血小板减少患病率较低��,但在后续实际研究中���,接受固定剂量(每12小时600mg)治疗超过10天的不同患者群体中���,患病率较高[3]���。
本研究中���,积极的TDM聚焦于将利奈唑胺Cmin控制在2-8mg/L���,对预防和恢复血小板减少有益��,即使是长期治疗���。A组和B1亚组患者血小板减少发生率远低于以往非干预性研究���。虽然有西班牙前瞻性单中心研究反对TDM的作用���,但该研究为非干预性���,且仅进行单次TDM评估���,与本研究不同���。
多变量回归分析表明���,利奈唑胺中位Cmin和基线血小板计数是与血小板减少风险独立相关的变量��。此前研究显示治疗时长与血小板减少风险有关[4]���,但本研究未发现此关联���,这与另一项干预性研究结果一致���,该研究发现对高风险患者降低利奈唑胺剂量可预防不良反应��。此外���,本研究发现���,短暂药物过量后将利奈唑胺Cmin稳定控制在目标范围���,有助于患者在不停药的情况下从血小板减少中恢复���。
本研究也存在局限性���,如缺乏对照组���、样本量较小��,无法明确利奈唑胺暴露与临床疗效的关系���,也不能排除联合用药作为混杂因素对血小板减少的影响���。不过���,前瞻性研究设计对评估长期治疗的安全性有一定优势���。
总体而言���,本研究表明积极的利奈唑胺TDM对预防和恢复剂量依赖性血小板减少有益���,使长期治疗的管理更安全可行���,为后续更大规模的前瞻性研究提供了初步数据��。

参考文献
1. Pea, F., et al., Therapeutic drug monitoring may improve safety outcomes of long-term treatment with linezolid in adult patients. J Antimicrob Chemother, 2012. 67(8): p. 2034-42.
2. Pea, F., P.G. Cojutti, and M. Baraldo, A 10-Year Experience of Therapeutic Drug Monitoring (TDM) of Linezolid in a Hospital-wide Population of Patients Receiving Conventional Dosing: Is there Enough Evidence for Suggesting TDM in the Majority of Patients? Basic Clin Pharmacol Toxicol, 2017. 121(4): p. 303-308.
3. Grau, S., et al., Linezolid: low pre-treatment platelet values could increase the risk of thrombocytopenia. J Antimicrob Chemother, 2005. 56(2): p. 440-1.
4. Kim, H.S., et al., Linezolid-induced thrombocytopenia increases mortality risk in intensive care unit patients, a 10 year retrospective study. J Clin Pharm Ther, 2019. 44(1): p. 84-90.